Hai Quipperian, bagaimana kabarnya? Semoga selalu sehat dan tetap semangat belajar, ya.
Quipperian pasti tahu kan jika setiap senyawa kimia memiliki sifat dan karakteristik yang berbeda-beda, misalnya NaCl dan KOH. Reaksi antara ion Na+ dan Cl– akan membentuk suatu garam, yaitu natrium klorida. Sementara itu, reaksi antara ion K+ dan OH– akan membentuk suatu basa yang disebut kalium hidroksida.
Apakah kedua senyawa memiliki persamaan? Tentu tidak ya, karena keduanya dibentuk oleh unsur yang berbeda. Bagaimana ilmuwan bisa tahu sifat-sifat dan macam-macam unsur? Keterangan lengkap tentang unsur biasa ditampilkan dalam bentuk SPU (sistem periodik unsur). Ingin tahu selengkapnya tentang sistem periodik unsur? Check this out!
Perkembangan Sistem Periodik Unsur
Adapun perkembangan sistem periodik unsur adalah sebagai berikut.
1. Pengelompokan oleh Antoine Lavoisier
Perkembangan sistem periodik unsur diawali pada tahun 1789 oleh Antoine Lavoisier. Pada tahun itu, Lavoisier berhasil mengelompokkan 33 jenis unsur berdasarkan sifat kimianya, misalnya gas, tanah, logam, dan nonlogam.
2. Pengelompokan unsur Triade Dobereiner
Pada tahun 1817, seorang kimiawan asal Jerman, Johann Wolfgang Dobereiner, berhasil mengelompokkan unsur-unsur berdasarkan kenaikan massa dan kesamaan sifatnya. Setiap kelompok terdiri dari tiga unsur. Itulah mengapa penemuannya dikenal sebagai Triade Dobereiner. Ketentuan dari triade ini adalah massa unsur yang di tengah merupakan rata-rata unsur awal dan akhirnya.
3. Pengelompokan unsur oktaf Newlands
Tampaknya, masih dari tanah Eropa ya Quipperian, tepatnya pada tahun 1864 seorang kimiawan asal Inggris, John Newlands, berhasil mengelompokkan unsur berdasarkan kenaikan massa atom relatif. Berdasarkan hasil penelitiannya, Newlands mendapati bahwa unsur kedelapan sifatnya mirip dengan unsur pertama, unsur kesembilan mirip dengan unsur kedua, dan seterusnya. Keunikan sifat yang seperti itulah kemudian disebut hukum oktaf. Kelemahan dari pengelompokkan oleh Newlands ini adalah hanya berlaku untuk unsur bermassa atom kecil.
4. Tabel periodik unsur Mendeleev dan Lothar Mayer
Hukum oktaf yang ditemukan oleh Newlands, mendorong ilmuwan asal Rusia dan Jerman, yaitu Dimitri Mendeleev dan Lothar Mayer, untuk meneliti kembali hubungan massa atom dan sifat kimia unsur. Penelitian keduanya fokus pada besaran yang berbeda. Mendeleev meneliti hubungan antara massa atom dan sifat-sifat kimia. Sementara itu, Mayer meneliti hubungan antara massa atom dan sifat-sifat fisika. Mendeleev berkesimpulan bahwa susunan unsur berdasarkan kenaikan massa atomnya akan menghasilkan perulangan sifat secara periodik. Pernyataan ini dikenal sebagai hukum periodik unsur. Pada tahun 1871, Mendeleev berhasil menerbitkan tabel periodik unsur dengan lajur tegak disebut golongan dan lajur mendatar disebut periode.
5. Tabel periodik modern (bentuk panjang)
Pada tahun 1914, Henry Moseley menyatakan bahwa sifat dasar atom itu terletak pada nomor atomnya, bukan nomor massanya. Dari serangkaian penelitian yang ia lakukan, Henry Moseley berhasil memperbarui tabel periodik unsur yang digagas oleh Mendeleev. Tabel periodik unsur milik Moseley terdiri dari dua lajur, yaitu lajur mendatar disebut periode dan lajur tegak disebut golongan. Tabel periodik Moseley inilah yang biasa kamu gunakan di pelajaran Kimia. Berikut ini contohnya!

Adapun ketentuan lajurnya adalah sebagai berikut.
a. Periode
Periode menunjukkan banyaknya kulit yang terisi elektron. Artinya, nomor periode sama dengan jumlah kulitnya. Jumlah periode yang ada di tabel periodik unsur adalah 7.
- Periode 1 termasuk periode pendek karena memuat 2 unsur.
- Periode 2 dan 3 termasuk periode pendek karena memuat 8 unsur.
- Periode 4 dan 5 termasuk periode panjang karena berisi 18 unsur.
- Periode 6 termasuk periode sangat panjang karena berisi 32 unsur.
- Periode 7 termasuk periode belum lengkap karena belum semua unsurnya ditemukan.
b. Golongan
Golongan disusun berdasarkan kemiripan sifat. Jumlah golongan yang ada di tabel periodik unsur adalah 8. Kedelapan golongan dibagai menjadi dua, yaitu golongan A (utama) dan B (transisi).
Menentukan Letak Periode dan Golongan Suatu Unsur
Bagaimana cara menentukan unsur dan golongan suatu unsur? Check this out!
1. Golongan A
Elektron terakhir unsur golongan A berada di subkulit s atau p. Jika elektron terakhirnya berada di subkulit s, nomor golongannya sama dengan jumlah elektron terakhirnya. Jika elektron terakhirnya berada di subkulit p, nomor golongannya jumlah elektron terakhir pada subkulit s dan p (s + p).
2. Golongan B
Unsur yang berada di golongan B memiliki elektron terakhir di subkulit d. Nomor golongannya ditentukan dari hasil penjumlahan elektron di subkulit s dan d. Perhatikan ketentuan berikut.
- s2 d1 -> golongan IIIB
- s2 d2 -> golongan IVB
- s2 d3 -> golongan VB
- s1 d5 -> golongan VIB
- s2 d5 -> golongan VIIB
- s1 d10 -> golongan IB
- s2 d10 -> golongan IIB
- s2 d5 s2 d7 s2 d8 -> golongan VIIIB
Perhatikan SUPER “Solusi Quipper” berikut ini.

3. Golongan transisi dalam (IIIB)
Golongan transisi dalam memiliki subkulit terakhir f. Contohnya lantanida di 4f dan aktinida di 5f.
Untuk lebih jelasnya, simak contoh soal berikut ini.
Contoh Soal 1
Tentukan letak periode dan golongan unsur IINa dan 17Cl!
Pembahasan:
Pertama, Quipperian harus menguraikan dulu kulit elektronnya.
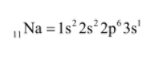
Oleh karena kulit tertinggi adalah kulit ke-3, maka unsur tersebut masuk dalam periode 3. Elektron terakhir berada di subkulit s dengan jumlah 1. Artinya, unsur tersebut masuk golongan IA
![]()
Oleh karena kulit tertinggi adalah kulit ke-3, maka unsur tersebut masuk dalam periode 3. Elektron terakhir berada di subkulit p dengan jumlah elektron valensi 7 (2 dari subkulit 3s dan 5 dari subkulit p). Artinya, unsur tersebut masuk golongan VIIA.
Jadi, unsur IINa dan 17Cl terletak di periode 3 dan golongan IA serta VIIA.
4. Elektron valensi
Elektron valensi adalah elektron yang berada di kulit terluar.

5. Kulit valensi
Kulit valensi menyatakan kulit tempat melekatnya elektron valensi.
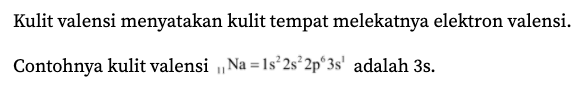
6. Blok
Blok menyatakan letak subkulit dari elektron valensi, misalnya s, (s+p), dan seterusnya.
Sifat Periodik Unsur
Adapun sifat keperiodikan unsur adalah sebagai berikut.
1. Jari-jari atom
Jari-jari atom merupakan jarak antara inti atom dan kulit terluarnya. Ketentuan yang berkaitan dengan jari-jari atom adalah sebagai berikut.
- Dalam satu golongan, semakin ke bawah jari-jari atomnya semakin besar. Hal itu karena jum;ah kulitnya semakin banyak. Contohnya, jari-jari atom K lebih besar daripada Li.
- Dalam satu periode, semakin ke kanan jari-jari atomnya semakin kecil. Hal itu karena jumlah kulitnya tetap, sedangkan muatan intinya semakin banyak. Contohnya jari-jari atom Na lebih besar daripada Cl.
- Jari-jari kation (ion positif) lebih kecil daripada atom netralnya. Contohnya jari-jari atom Na lebih besar daripada Na+.
- Jari-jari anion (ion negatif) lebih besar daripada atom netralnya.
2. Energi ionisasi
Energi ionisasi adalah energi yang dibutuhkan untuk melepaskan satu elektron pada atom netral dalam bentuk gas. Dalam satu periode, semakin ke kanan, energi ionisasi akan semakin besar. Sementara itu, dalam satu golongan, semakin ke bawah energi ionisasi semakin kecil. Namun, ketentuan tersebut tidak berlaku untuk unsur periode 3 seperti Mg, Al, P, dan S.
3. Afinitas elektron
Afinitas elektron adalah energi yang dilepaskan oleh atom gas untuk berubah menjadi ion negatif. Dalam satu periode, semakin ke kanan, afinitas elektron semakin besar. Dalam satu golongan, semakin ke bawah, afinitas elektron semakin kecil.
4. Keelektronegatifan
Keelektronegatifan adalah kecenderungan suatu atom untuk menarik elektron. Dalam satu periode, semakin ke kanan keelektronegatifannya semakin besar. Dalam satu golongan, semakin ke bawah keelektronegatifannya semakin kecil.
Nah, untuk mengasah pemahamanmu tentang sistem periodik unsur, yuk simak contoh soal berikut ini.
Contoh Soal 2
Unsur X memiliki bilangan kuantum elektron terakhir sebagai berikut.
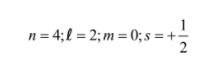
Jika jumlah neutron dari atom X adalah 4s, tentukan periode dan golongan unsur X tersebut!
Pembahasan:
Bilangan kuantum elektron terakhir dari unsur X adalah sebagai berikut.
- n = 4 -> kulit ke-4
- l = 2 -> subkulit d
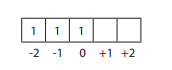
- m = 0 -> elektron terakhir di orbital 0
- s = +1/2 -> elektron ke arah atas
Dengan demikian, diperoleh:
Konfigurasi elektronnya:
X = 1s2 2s2 2p6 3s2 3p6 4p6 3d10 4p6 5s2 4d3
Berdasarkan konfigurasi di atas, diketahui bahwa
- Kulit tertinggi berada di kulit ke-5. Artinya, unsur X termasuk periode 5.
- Elektron terakhirnya berada di subkulit d dan jumlah elektron valensinya 5, yaitu 2 elektron dari subkulit 5s dan 3 elektron dari subkulit 4d. Artinya, unsur X termasuk golongan VB.
Jadi, unsur X masuk dalam periode 5 dan golongan VB.
Contoh Soal 3
Jika konfigurasi ion X3+ = [Ar] 3d5, tentukan konfigurasi atom X!
Pembahasan:
Konfigurasi ion X3+ = [Ar] 3d5
Pada ion X3+, ada 3 elektron yang keluar dari atom X, yaitu 2 elektron berasal dari subkulit 4s dan 1 elektron berasal dari subkulit 3d. Dengan demikian, jika atom X memiliki elektron lengkap, konfigurasinya menjadi X = [Ar] 4s2 3d6.
Itulah pembahasan Quipper Blog tentang sistem periodik unsur. Jika Quipperian belum puas dengan pembahasan kali ini, silakan tonton video pembahasannya di Quipper Video, ya. Jadikan Quipper Video sebagai mitra belajar yang menyenangkan. Salam Quipper!
Penulis: Eka Viandari