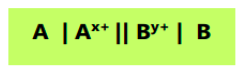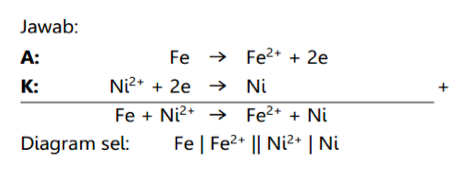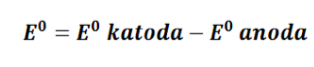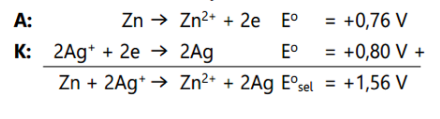Sel volta merupakan sel yang mengubah energi kimia jadi energi listrik. Ada 2 jenis elektroda dalam sel volta; elektroda padat dan elektroda tidak padat. Ada pula istilah deret volta, yakni deret kereaktifan logam yang memberitahu nilai potensial elektroda standar logam. Dalam praktiknya, sel volta menggunakan reaksi redoks (reduksi dan oksidasi) spotan.
Halo Quipperian! Kali ini Quipper Blog akan membahas tentang materi sel volta. Materi sel volta sering keluar dalam Ujian Semester kelas 12 atau pun soal UNBK Kimia. Namun, sebagian dari siswa masih kesulitan menjawab soal tersebut karena kurangnya memahami materi sel volta secara mendalam.
Nah, makanya pada sesi kali ini, Quipper Blog akan membahas tentang sel volta dan diagramnya, prinsip kerja sel volta, sifat deret volta, tips dan trik menyelesaikan soal sel volta, serta soal dan pembahasan dari bank soal Quipper Video yang up to datetentunya. Check this out!
Pengertian Sel Volta

Sel volta adalah sel yang mengubah energi kimia menjadi energi listrik. Sel volta menggunakan reaksi redoks spontan. Reaksi redoks merupakan singkatan dari reaksi reduksi dan oksidasi. Gambar dan prinsip kerja dari sel volta adalah sebagai berikut:
Hasil reaksi pada sel volta ditulis menggunakan diagram sel volta. Diagram selnya adalah sebagai berikut:
Di mana:
A adalah logam anoda
Ax+ adalah ion logam anoda yang teroksidasi
By+ adalah ion logam katoda yang tereduksi
B adalah ion logam katoda.
Tanda ( | | ) adalah jembatan garam
Tanda ( | ) adalah reaksi yang terjadi pada elektroda
Contoh: Pada suatu sel volta, anoda besi tercelup pada FeSO4, katoda nikel tercelup pada NiSO4. Buatlah reaksi sel volta dan diagram selnya!
Jenis-jenis Elektroda pada Sel Volta

Jenis-jenis elektroda pada sel volta adalah sebagai berikut.
a. Elektroda padat/logam
Logam padat dijadikan elektroda dan bereaksi. Contoh elektroda Fe pada larutan FeSO4, elektroda Ni pada larutan H2SO4.
b. Elektroda tidak padat
Apabila elektroda merupakan elektroda inert (tidak mudah bereaksi) (Pt, Au, dan C), maka zat lainlah yang mengalami reaksi sel.
Nilai Potensial Sel Standar
Suatu sel volta memiliki nilai potensial sel standar (E0 sel). Rumusan matematis dari potensial standarnya adalah sebagai berikut:
Contoh soal: Tentukan nilai potensial sel jika anodanya adalah Zn dengan E0 = -0,76 V, dan katodanya adalah Ag dengan E0= + 0,80 V.
Jawab:
Diketahui E0Anoda = -0,76 V dan E0katoda = 0,80 Volt
Sehingga nilai potensial selnya adalah sebagai berikut:
Maka diagram sel volta yang dihasilkan adalah sebagai berikut:
Nilai potensial standar ini menunjukkan 3 ciri pada sel volta:
- Tegangan yang dihasilkan oleh sel volta
- Jika nilai E0sel > 0 (+) maka reaksi sel spontan (berlangsung)
- Jika nilai E0sel < 0 (-) maka reaksi sel tidak spontan (tidak berlangsung)
Reaksi Sel tidak spontanmenunjukkan tidak terjadinya suatu reaksi pada sel volta. Hal ini disebabkan karena penempatan anoda dan katoda tidak mengacu pada deret volta, sehingga E0 sel bernilai negatif.
Deret Volta
Deret Volta adalah deret elektrokimia/kereaktifan logam yang menunjukkan nilai potensial elektroda standar logam (E0). Sifat deret volta adalah sebagai berikut:
- Semakin ke kanan, nilai logam semakin mudah tereduksi (Nilai E0lebih positif)
- Semakin ke kiri, nilai logam semakin mudah teroksidasi (Nilai E0lebih negatif)
Di bawah unsur-unsur deret volta terdapat nilai kereaktifan logam. Untuk menjawab soal-soal Kimia SMA, kita tidak perlu menghafal nilai kereaktifan logam tersebut. Kita hanya perlu memahami posisi dari unsur-unsur pada deret volta. Deret volta dimulai dari kiri ke kanan, di mana unsur kiri nilainya lebih negatif (-) menuju ke unsur yang nilainya lebih positif (+).
Untuk lebih mudah menghafal unsur-unsur dari deret volta, Quipper Blog menyediakan jembatan keledai yang menarik agar Quipperian semakin mudah menghafalnya yaitu sebagai berikut:

Tips Mengerjakan Soal Materi Sel Volta

Dalam penyelesaian soal sel volta, biasanya terdapat 3 jenis soal yang diberikan. Berikut solusi yang Quipper Blog bisa berikan buat kamu:
a. Penentuan unsur yang tepat pada sel volta
Untuk menyelesaikan soal ini, Quipperian harus memahami bahwa posisi katoda adalah sebelah kanan sedangkan anoda berada di sebelah kiri. Katoda memiliki potensial yang besar sedangkan anoda memiliki potensial yang kecil. Oleh sebab itu, dapat dibuat jembatan keledai sebagai berikut:

b. Penetuan logam elektroda sel volta yang tepat
Untuk menyelesaikan soal tipe ini, Quipperian harus memahami bahwa syarat terjadinya sel volta adalah reaksinya spontan, artinya elektrodanya mempunyai nilai positif. Ingat lagi rumus matematis elektroda standar, ya!
c. Penentuan logam yang tepat saat terjadinya proses pengorosian logam
Korosi (perkaratan)adalah suatu reaksi reduksi-oksidasi antara logam dengan faktor lingkungannya. Mekanisme terjadinya korosi secara umum adalah:
- logam menjadi anoda dan teroksidasi
- faktor lingkungan menjadi katoda dan tereduksi
Proses korosi akan cepat terjadi apabila logam tersebut dilapisi dengan logam yang berada pada sebelah kanan di deretan voltanya. Contoh Fe (Besi) akan cepat korosi apabila dilapisi logam Ni (Nikel), Pb (timbal), Pt (platina), dan lainnya.
Contoh Soal Materi Sel Volta

Biar kamu makin dalam belajar tentang sel voltanya, coba yuk kerjakan contoh soal dari Quipper Video yang ada di bawah ini.
Contoh Soal 1

Pembahasan:
Dari soal 1 terlihat bahwa terdapat 5 unsur logam yang memiliki potensial yang berbeda-beda. Diketahui nilai potensial unsur Ag+= +0,79 V sedangkan nilai potensial unsur Mg adalah -2, 35V. Dari soal terlihat bahwa unsur Ag berperan sebagai katoda dan unsur Mg berperan sebagai anoda. Maka diperoleh nilai potensial elektrodanya sebagai berikut:

Contoh Soal 2

Pembahasan:
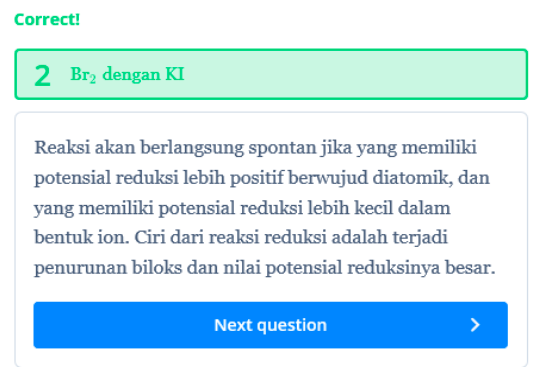
Diketahui 4 unsur yang memiliki potensial yang berbeda-beda. Pertanyaan dari unsur tersebut reaksi yang dapat berlangsung spontan adalah?
Reaksi sel volta dapat berlangsungspontanapabila nilai elektroda mempunyai nilai positif (+). Oleh sebab itu menggunakan rumus matematis elektroda dan diperoleh reaksi antara Br2dan KI karena nilai Elektrodanya (E0) = +0,45 V.
Contoh Soal 3

Pembahasan:
Dari soal diatas, terdapat beberapa unsur yang memiliki potensial yang berbeda, ada yang (+) dan ada yang (-). Pertanyaannya adalah urutan yang tepat pada deret volta dari kiri ke kanan adalah…
Sebagaimana kita ketahui bahwa deret Volta adalah suatu deretan unsur yang memiliki potensial yang berbeda dimana dari kiri dimulai dari elektroda yang negatif (-) menuju elektroda yang nilainya positif (+). Oleh sebab itu jawaban yang tepat dari soal no 3 adalah sebagai berikut.

Gimana Quipperian pembahasan materi sel volta dari Quipper Blog di atas? Mudah-mudahan cukup membantu dan mencerahkan kamu, ya! Anyway, kalau kamu masih mau lanjut belajar materi ini atau materi lainnya, langsung saja gabung di Quipper Video, deh. Di sana kamu bisa belajar materi apapun dari para tutor kece lewat video, rangkuman, dan latihan soal. Buruan daftarkan diri dan sampai jumpa di artikel lainnya, ya!
Sumber:
- Wardaya College.Aolikasi Elektrokimia. Jakarta : Wardaya College.
- Zulfikar. 2008. Kimia untuk Kesehatan. Kemdikbud : Jakarta
- https://materi78.files.wordpress.com/2013/06/volta_kim2_4.pdf
Penulis: William Yohanes