Atom pertama kali lahir dari filsafat antara Democritus dengan Aristoteles. Ada beberapa teori model atom, diantaranya teori model atom Dalton, Thomson, Rutherford, dan Bohr. Model atom Bohr merupakan teori yang paling banyak dimanfaatkan, salah satunya untuk penemuan tabel unsur periodik.
Halo Quipperian! Kali ini Quipper Blog akan membahas hal yang menarik lho, yaitu “Sejarah Perkembangan Teori Model dan Struktur atom”. Teori model dan struktur atom berkembang pada awal abad ke-19. Hal tersebut dipengaruhi dengan keingintahuan para ilmuwan tentang apa yang menjadi penyusun dari suatu materi dan berkembangnya metode ilmiah dalam pembuktian sains.
Nah, pada sesi kali ini, Quipper Blog akan membahas tentang jenis-jenis model atom (Dalton, Thomson, Rutherford, dan Bohr), eksperimen yang mendukung model atom mereka, serta struktur atom dari hasil model atom Bohr. Let’s check this out!
Gagasan tentang Atom Pertama Kali

Gagasan pertama kali tentang model atom lahir dari filsafat antara Democritus dan Aristoteles (500 Sebelum Masehi). Ada perbedaan filsafat di antara mereka tentang penyusun dari suatu materi. Aristoteles menyatakan bahwa suatu materi tersusun dari suatu materi kecil yang dapat dibagi terus-menerus. Sedangkan Democritus menyatakan bahwa materi tersusun dari suatu partikel yang disebut atomos (atomos adalah partikel kecil yang tidak dapat dibagi-bagi lagi (bahasa Yunani)).
Namun karena merupakan filsafat, pengetahuan tentang atom tidak berkembang karena hal tersebut tidak dapat dibuktikan secara ilmiah. Pengetahuan tentang atom mulai berkembang pesat sejak penelitian John Dalton dan Avogadro yang mengungkapkan suatu gas yang berbeda namun memiliki volume yang sama dan berisi jumlah molekul yang sama bila suhu dan tekanannya sama.
Teori-teori model dan struktur atom tersebut mulai disempurnakan karena memiliki kekurangan sehingga dihasilkan teori model atom Thomson, teori model atom Rutherford, dan teori model atom Bohr.
Teori Model Atom Dalton

Teori model atom Dalton pertama kali muncul pada tahun 1808. Teori ini muncul dari penelitian berat gabungan secara kimia Dalton menyimpulkan bahwa bentuk dan struktur atom menyerupai bola pejal yang padat. Selain itu, berdasarkan penelitian yang dipublikasikan dalam A New System of Chemical Philosophy, Dalton menyimpulkan sifat-sifat atomnya adalah sebagai berikut:
- Materi terdiri atas atom yang tidak dapat dibagi lagi.
- Semua atom dari unsur kimia tertentu memiliki massa dan sifat yang sama.
- Unsur kimia yang berbeda akan memiliki jenis atom yang berbeda.
- Selama reaksi kimia, atom-atom hanya dapat bergabung dan dipecah-pecah menjadi atom-atom yang terpisah, tetapi atau tidak dapat diubah selama reaksi kimia tersebut.
- Suatu senyawa terbentuk dari unsur-unsurnya melalui penggabungan atom tidak sejenis dengan perbandingan yang sederhana.
Teori Model Atom Thomson

Teori model atom Thomson lahir dari percobaan Joseph John Thomson tahun 1897. J.J. Thomson melakukan percobaan menggunakan tabung sinar katoda. Berdasarkan hasil penelitiannya, terdapat atom yang memiliki muatan negatif yang disebut elektron.
Oleh sebab itu, J.J. Thomson mengusulkan bahwa model atom yang tepat adalah seperti roti kismis. Menurut Thomson, model atom berbentuk seperti bola kismis dengan muatan listrik terdistribusi merata dan elektron tersebar pada bola ini dengan jumlah muatan negatif yang sama dengan muatan positif.
Teori Model Atom Rutherford
Teori model atom Rutherford lahir dari percobaan Ernest Rutherford (1871-1937) bersama murid-muridnya, Hans Geiger dan Ernest Mandem. Percobaan mereka adalah memberikan hamburan partikel α pada suatu lapisan logam tipis emas.
Dari hasil eksperimen tersebut, mereka menemukan bahwa sebagian besar partikel α melewati lapisan tipis seperti menembus ruang kosong dan ada juga partikel yang terdefleksi dengan sudut yang lebar. Eksperimen mereka juga menunjukkan bahwa ada partikel yang terpantul kembali ke arah datangnya sinar.
Kemudian Rutherford menjelaskan hasil eksperimennya dengan menggunakan model atomnya bahwa terdapat muatan positif dalam sebuah atom terkonsentrasi pada suatu bagian relatif kecil dibanding ukuran atom. Bagian bermuatan positif ini disebut inti (Nucleus) sedangkan bagian atom yang berada di luar dan bergerak mengelilingi inti atom seperti planet-planet mengelilingi matahari disebut Elektron.
Teori Model Atom Bohr

Teori Model atom Bohr lahir dari gagasan Niels Bohr (1913). Teori model atom Bohr merupakan penyempurnaan dari model atom Ruhterford yang gagal menjelaskan gaya gerak elektron pada lintasan orbit. Bohr mengusulkan bahwa:
- Elektron-elektron yang bergerak di dalam orbit memiliki momentum dan energi yang terkuantisasi sehingga hanya beberapa orbit yang yang berada pada jarak dari inti.
- Elektron-elektron tidak akan kehilangan energi secara perlahan-lahan saat mereka bergerak di dalam orbit melainkan akan tetap stabil di dalam sebuah orbit yang tidak meluruh.
Dua poin tersebut diberikan sebagai penyempurnaan dari model atom Rutherford di mana model atom tersebut masih memakai kerangka hukum Newtonian (Fisika Klasik). Berbeda dengan Bohr yang mengesampingkan Hukum Newtonian dan menggunakan hukum mekanika modern.
Hukun Newtonian dipakai saat pergerakan kecepatan benda masih kecil. Hukum Mekanika modern digunakan saat pergerakan kecepatan partikel hampir mendekati kecepatan cahaya ( V = 3 x 10 8 m/s).
Model atom Bohr merupakan model atom yang paling sering dipakai karena sederhana tetapi dapat menjelaskan banyak hal. Salah satu kesuksesan dari model atom Bohr adalah lahirnya tabel periodik unsur-unsur.
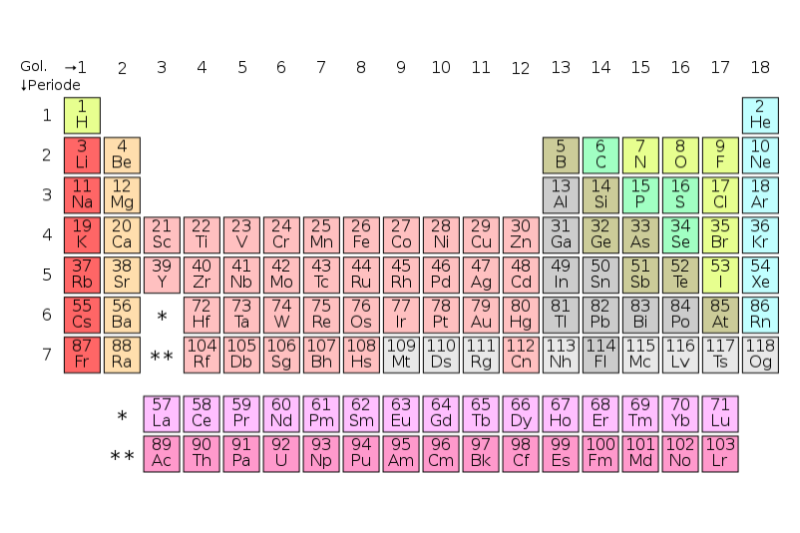
Tabel periodik unsur-unsur adalah sebuah tabel yang berisi atom-atom yang penggolongan terhadap sifat dan jenis-jenisnya (contohnya unsur logam, non-logam, padat, gas, cair, atau unsur buatan). Istilah lain yang sering digunakan untuk menyatakan jenis atom adalah unsur.
Coba Quipperian cek gambar tabel periodik di bawah ini, deh. Dapat ditunjukkan unsur warna merah maroon termasuk golongan logam, sedangkan unsur yang berwarna hijau termasuk golongan gas, dan juga ada yang termasuk unsur di golongan lantanida dan aktinida (berwarna cokelat muda dan cokelat tua), unsur ini termasuk unsur yang dibuat oleh manusia sendiri.
Jenis atom yang sama akan mempunyai jumlah proton yang sama. Sebaliknya atom yang berbeda memiliki jumlah proton yang berbeda. Contohnya unsur hidrogen (H) mempunyai sebuah proton 1 sedangkan unsur emas (Au) mempunyai 79 buah proton.
Berdasarkan perjanjian, setiap jenis atom diberi nomor – yang disebut sebagai nomor atom yang ditentukan berdasarkan jumlah proton yang dimilikinya. Sebagai contoh, nomor atom unsur unsur hidrogen adalah 1 sedangkan nomor atom dari unsur emas adalah 79. Jenis-jenis atom tersebut dapat dilihat pada tabel periodik unsur-unsur.
Struktur Atom
Gagasan dari model atom Bohr memudahkan kita untuk memahami struktur atom. Sebagaimana yang sudah dijelaskan bahwa atom terdiri dari 3 jenis partikel penyusun yaitu Elektron (partikel bermuatan negatif (-)), Proton (partikel bermuatan positif (+)), dan Neutron (partikel tidak bermuatan). Atom terdiri dari dari bagian inti atom (proton + neutron) dan bagian luar (elektron). Besaran muatan listrik dan massa dari struktur atom ini dijelaskan pada tabel di bawah ini.
| Partikel | Muatan listrik | Massa | ||
| Coulomb | Elementer | Kg | Sma* | |
| Elektron | -I,6 x 10 -19 | -1 | 9,1 x 10-31 | 0 |
| Proton | +1,6 x 10 -19 | +1 | 1,67 x 10-27 | 0 |
| Neutron | 0 | 0 | 1,67 x 10-27 | 1 |
*sma adalah satuan dari massa atom
So, Quipperian gimana materi pembahasan mengenai teori model dan struktur atom di atas? Semoga cukup membantu kamu, ya! Kalau kamu masih mau lanjut belajar, gabung saja dengan Quipper Video. Di sana kamu akan diajar oleh para tutor kece lewat video, rangkuman, dan latihan soal. Cusss, daftar ya!
Sumber:
- BATAN. Buku Pintar Nuklir. Tangerang : Batan Publisher.
- Niyata Sirat. Struktur atom. Jakarta:Kemdikbud
- https://id.wikipedia.org/wiki/Model_Bohr
Penulis: William Yohanes